Page 187 - A. Doadrio: Quimica Inorganica
P. 187
Silicio,
germanio,
estaño
y
plomo
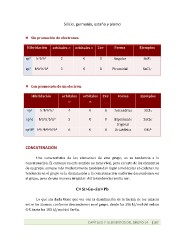
n Sin
promoción
de
electrones.
Hibridación
orbitales
σ
orbitales
π
2xe-‐
Forma
Ejemplos
sp2
h2h1h1
2
0
1
Angular
SnF2
sp3
h2h1h1h0
3
0
1
Piramidal
SnCl3-‐
n Con
promoción
de
un
electrón.
Hibridación
orbitales
orbitales
2xe-‐
Forma
Ejemplos
σ
π
SiCl4
sp3
h1h1h1h1
4
0
0
Tetraédrica
SnCl5-‐
SiF62-‐
sp3d
h1h1h1h1h0
5
0
0
Bipirámide
sp3d2
h1h1h1h1h0h0
6
trigonal
0
0
Octaédrica
CONCATENACIÓN
Una
característica
de
los
elementos
de
este
grupo,
es
su
tendencia
a
la
concatenación.
El
carbono
en
este
sentido
no
tiene
rival,
pero
el
resto
de
los
elementos
de
su
grupo,
aunque
más
modestamente
también
dan
lugar
a
moléculas
en
cadenas.
La
tendencia
en
el
grupo
es
la
disminución
a
la
concatenación
conforme
descendemos
en
el
grupo,
pero
de
una
manera
irregular.
Así
la
tendencia
resulta
ser:
C» Si>Ge~Sn» Pb
Lo
que
sin
duda
tiene
que
ver
con
la
disminución
de
la
fuerza
de
los
enlaces
entre
los
átomos,
conforme
descendemos
en
el
grupo,
desde
los
356
kJ/mol
del
enlace
C-‐C
hasta
los
105
kJ/mol
del
Sn-‐Sn.
CAPÍTULO
7:
ELEMENTOS
DEL
GRUPO
14
|187
germanio,
estaño
y
plomo
n Sin
promoción
de
electrones.
Hibridación
orbitales
σ
orbitales
π
2xe-‐
Forma
Ejemplos
sp2
h2h1h1
2
0
1
Angular
SnF2
sp3
h2h1h1h0
3
0
1
Piramidal
SnCl3-‐
n Con
promoción
de
un
electrón.
Hibridación
orbitales
orbitales
2xe-‐
Forma
Ejemplos
σ
π
SiCl4
sp3
h1h1h1h1
4
0
0
Tetraédrica
SnCl5-‐
SiF62-‐
sp3d
h1h1h1h1h0
5
0
0
Bipirámide
sp3d2
h1h1h1h1h0h0
6
trigonal
0
0
Octaédrica
CONCATENACIÓN
Una
característica
de
los
elementos
de
este
grupo,
es
su
tendencia
a
la
concatenación.
El
carbono
en
este
sentido
no
tiene
rival,
pero
el
resto
de
los
elementos
de
su
grupo,
aunque
más
modestamente
también
dan
lugar
a
moléculas
en
cadenas.
La
tendencia
en
el
grupo
es
la
disminución
a
la
concatenación
conforme
descendemos
en
el
grupo,
pero
de
una
manera
irregular.
Así
la
tendencia
resulta
ser:
C» Si>Ge~Sn» Pb
Lo
que
sin
duda
tiene
que
ver
con
la
disminución
de
la
fuerza
de
los
enlaces
entre
los
átomos,
conforme
descendemos
en
el
grupo,
desde
los
356
kJ/mol
del
enlace
C-‐C
hasta
los
105
kJ/mol
del
Sn-‐Sn.
CAPÍTULO
7:
ELEMENTOS
DEL
GRUPO
14
|187